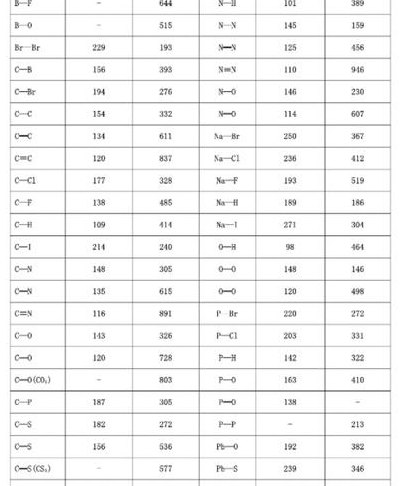
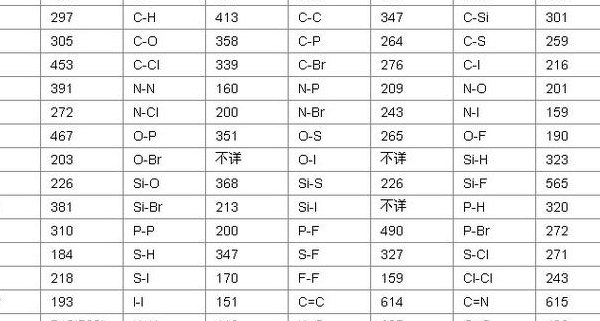
键能越大(键能越大越容易断裂吗)
键能越大越稳定吗
越小越稳定。它本身所具有的能量则与之不同,它本身所具有的能量越大,说明他和其他物质反应的能力越强,所以,它本身所具有的能量越大,它越不稳定。而键能是指破坏1mol化学键所需要的能量,因此,键能越大,说明破坏之所需要的能量越大,他就越不容易被破坏。
键能越小,表明断裂该键时需要输入的能量较少,因此键越不稳定。 相反,键能越大,意味着断裂该键需要输入较多的能量,键越稳定。 物质的能量水平不能直接通过键能来确定,键能反映的是物质与其分解产物之间的能量差。
②知识点运用:键能可以用于预测分子的稳定性,即键能越大的化合物一般比键能小的化合物更加稳定。③知识点例题讲解:举个例子,氢气和氧气可以发生反应生成水。在此反应中,氧气的键能比氢气高,因此氢气分子会被氧气分子的氧原子吸引到一起,形成一个更稳定的水分子。这就说明,键能越大,物质越稳定。
键级键长键能的大小关系
1、键级越大,键长越短,键能越大 键能一般和键长成反比。一般来说键能大,破坏该键就困难,物质就稳定。但是也不是绝对的,例如乙烷中的碳碳键的键能比乙烯中碳碳键键能小,但是乙烷却更稳定。键级又称键序,是分子轨道法中表示相邻的两个原子成键强度的一种数值。
2、键级的大小关系决定了键的长度和键的能量。一般来说,键级越高,键长越短,键能也就越大。键能通常与键长成反比,这意味着键能越大,键越稳定,破坏这样的键也就越困难,物质因此更加稳定。然而,这种关系并不是绝对的。
3、呈正相关关系。键级越高,键能越大,表示键的稳定性越高。相反,键级越低,键能越小,表示键的稳定性较低,在相同类型的键之间比较,键级、键能与1/键长呈正相关。这意味着,键长越短,键级和键能越大。
怎样理解物质的键能越大,能量越低,稳定性越强
1、键能的概念是衡量分子中化学键强度的一个重要指标。它定义为将分子中的化学键完全断裂所需的能量。键能越大,意味着要将化学键完全断裂需要的能量越多,因此化学键也就越稳定。从能量角度来看,键能越大,分子处于更低的能量状态,即能量越低,稳定性越强。
2、物质的键能指的是断裂这根键所需的能量,如果键能越大,那么所需的能量就越大,那么反应就难发生,物质的化学性质就越稳定。能量越低也是这个道理,能量低,那么达到活化状态所需的能量就越多,那么反应就难发生,物质的化学性质就越稳定。键能(Bond Energy)是从能量因素衡量化学键强弱的物理量。
3、键能的定义:键能是指拆开一摩尔共价键所消耗的能量或形成一摩尔共价键所释放的能量。它表示由共价键形成的物质内部原子之间结合的牢固程度。键能越大,破坏该分子需要外界提供的能量就越多,这表明分子内部原子之间的结合越牢固。 能量的高低指的是物质运动时所具有的能量。
键能越大物质越稳定吗
1、能量越低,物质越稳定;键能越大,物质越稳定。 键能的定义:键能是指拆开一摩尔共价键所消耗的能量或形成一摩尔共价键所释放的能量。它表示由共价键形成的物质内部原子之间结合的牢固程度。键能越大,破坏该分子需要外界提供的能量就越多,这表明分子内部原子之间的结合越牢固。
2、在化学领域,通常来说,键能(bond energy)越大,反应物质的稳定性越高。较强的化学键意味着更多的能量需要被输入才能破坏该键,因此反应物质更难被分解或转化为其他物质。这里的键能不是键具有的能量,是成键放出的能量或者是断键需要的能量。
3、键能越大确实可以意味着物质越稳定,但这需要结合具体的情况来看。在化学中,化学键是连接原子的力,能量单位通常是焦耳(J)或千焦耳(kJ)。如果一种化学键的键能较大,意味着在形成这种键时需要消耗更多的能量,这样的化学键在断裂时会释放更多的能量。