水分子的键角是的简单介绍
甲烷氨气和水的键角
1、甲烷分子中,四个碳氢键等长,每个碳氢键之间的夹角均为109°28′。氨气分子中,两个氮氢键之间的夹角为107°18′。水分子的两个氧氢键之间的夹角为105°。这些分子的空间结构可以通过键角来描述,键角是共价键方向性的体现,与分子的形状有直接关系。
2、在高中化学学习中,键角的知识常常以死记硬背的形式呈现,例如水分子的键角为105°,氨气为107°18’,甲烷为109°28’,二氧化碳为180°,硼三氟化物为120°。
3、甲烷是正四面体型结构,键角是109°28′;氨气是三角锥形结构,键角是107°;水时V形结构,键角是105°;CO 2 是直线型结构,键角是180°,答案选D。点评:该题是基础性试题的考查,难度不大。该题的关键是熟练记住常见分子的空间构型和键角大小,有利于调动学生的学习兴趣和学习积极性。
键角是怎样形成的比如水分子,为什么两个o
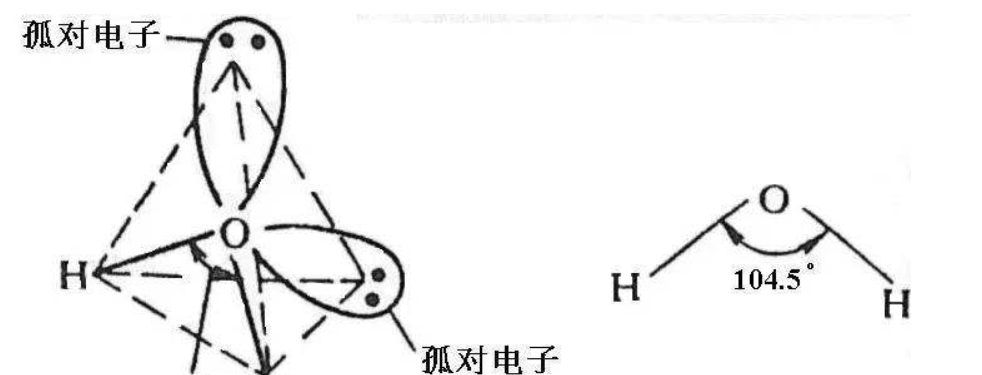
1、水分子中O有两对孤对电子,氨分子中N有1对孤对电子,斥力不一样导致键角也不一样。
2、水分子的键角是105度。水分子是H2O,折线型分子,水的键角是两个H-O键的夹角,因为水分子只形成了两个H-O键,不能计算孤对电子的夹角性状。键角是指在分子中,一个原子与其他两个原子形成的两个化学键之间的夹角叫做键角。键角是反映分子空间结构的重要因素之一。
3、H2O是水的分子式,氧原子价电子有6个,两对成对电子,两个单电子,与两个氢原子形成共价键。水的结构式为H-O-H,通过两对共用电子对形成两个O-H共价键,O原子还有两对孤对电子,所以H-O-H的空间构型是V形结构,键角∠HOH=105°。
4、水分子的分子形状是由于电子对的空间排布所决定的。在水分子中,氧原子周围有两对非共享电子对和两个氢原子。根据电子对排斥理论,非共享电子对之间的排斥力比共享电子对之间的排斥力更强,因此非共享电子对会占据较大的空间。这种电子对的空间排布导致氢原子之间的键角变小,接近109度28分。
水的键角是多少度
水分子的键角是105度。水分子是H2O,折线型分子,水的键角是两个H-O键的夹角,因为水分子只形成了两个H-O键,不能计算孤对电子的夹角性状。键角是指在分子中,一个原子与其他两个原子形成的两个化学键之间的夹角叫做键角。键角是反映分子空间结构的重要因素之一。
该物质键角为105°。水的键角之所以是105°,是因为水分子中的两个氢原子并不位于同一平面内,这种结构使得水分子具有更多的“极性”,这也是水分子之间能形成氢键的原因。同时,水的键角与水的溶解性和反应性有关,因为它影响了水分子与其他分子之间的相互作用。
总而言之,水分子的键角为109度28分是由于电子对排斥理论所引起的,它使得电子对和氢原子之间的空间排布最优化,从而使得键角变得较小。
水分子中两个H—O键之间的夹角是105°;一组S-O-S键的键角为109°28硫酸根中,一个O形成4个相同的S-O键,键与键之间斥力相同,键角均相同;水中两个H-O键,两个孤对电子,孤对电子对H-O键的斥力更大,所以导致两个H—O键之间的夹角小于均角。
负离子水的水分子的结构
习惯上我们把小于10个水分子缔合而成的水分子团称为小分子团,把大于10个水分子缔合而成的水分子团称为大分子团,负离子水就属于小分子团水。若干水分子通过氢键作用而聚合在一起,形成水分子团。液态水由分子团(簇)的形态存在。
自来水通常由13个水分子构成,而纯净水可能包含30到40个水分子,乡间死潭水的分子团则更大,可达200至300个。根据分子团的大小,我们将其分为小分子团(小于10个水分子)和大分子团(大于10个水分子)。负离子水就属于小分子团水,因其氢键结构更有利于人体吸收和利用。
水分子是主链状结构,如果不经常受到撞击,也就是说水不经常处于运动状态,而是静止状态时,这种链状结构就不断扩大、延伸,就变成俗称的“死水”,这就是衰老了的老化水。水的退化就是指水分子结构发生异常变化,水分子团变大,振频与波动异常,这些变化引起水自净功能和抗污染能力降低。