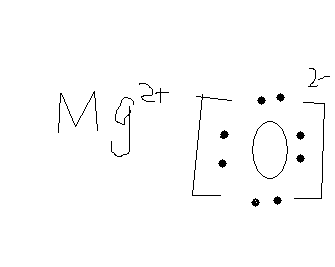氢氧化镁电子式(氢氧化镁电子结构)
氢氧化镁电子式
氢氧化镁的电子结构是指氢氧化镁分子中镁和氧原子的电子排布方式。氢氧化镁分子由一个镁离子和两个氧离子组成,其电子结构在化学反应和物理性质中起着重要作用。
镁的原子结构
镁的原子序数为12,其原子结构为1s2 2s2 2p6 3s2。这意味着镁原子的第一能级有2个电子,第二和第三能级分别有8个电子和2个电子。镁原子的外层电子结构为3s2,这使其易于与氧原子形成化合物。
氧的原子结构
氧的原子序数为8,其原子结构为1s2 2s2 2p4。氧原子的外层电子结构为2s2 2p4,这意味着它会倾向于接受电子以达到稳定的8个外层电子结构。氧原子与镁原子结合时,会与镁原子共享电子或接受镁原子的电子来形成稳定的化合物。
氢氧化镁的电子结构
在氢氧化镁分子中,镁离子失去了两个电子,其电子结构变为1s2 2s2 2p6。而氧离子各自获得了两个电子,其电子结构变为1s2 2s2 2p6。因此,在氢氧化镁中,镁离子带有2个正电荷,氧离子带有各自的负电荷。
化学性质影响
氢氧化镁的电子结构使其具有一系列特殊的化学性质。首先,由于镁离子失去了两个电子,它倾向于与带有2个电子的阴离子形成稳定的盐类化合物。其次,氧离子接受了两个电子,使其倾向于与带有两个空位的阳离子结合。这些特性使氢氧化镁在许多化学反应中发挥着重要作用。
物理性质影响
氢氧化镁的电子结构还影响着其物理性质。由于氧离子与镁离子间的电荷吸引力,氢氧化镁分子具有一定的结晶性和热稳定性。这使其在高温下能保持结构稳定,从而可以用作耐火材料。
结语
氢氧化镁的电子结构对其化学反应和物理性质产生了重要影响。通过了解氢氧化镁分子的电子排布方式,我们能更好地理解它的性质和用途,并在工业生产和科学研究中发挥作用。