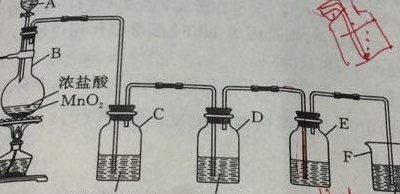
二氧化铅(二氧化铅和浓盐酸反应)
二氧化铅能氧化水吗
二氧化铅能氧化水。二氧化铅是一种强氧化剂,具有很强的氧化性,能与许多化学物质发生氧化反应。当二氧化铅与水反应时,会生成过氧化氢等物质,从而起到氧化水的作用。二氧化铅常用于染料、火柴、焰火、合成橡胶、电极等制造,也可用作氧化剂。
在溶解性方面,二氧化铅并不溶于我们常见的水和醇,但有趣的是,它能够溶于乙酸和氢氧化钠的水溶液中,这显示出其在特定溶剂中的可溶性特性。在加热条件下,二氧化铅的化学性质更为活跃。在290℃时,它会发生分解,生成氧气和三氧化二铅,温度进一步升高,还会生成四氧化三铅。
二氧化铅是一种棕黑色的结晶。二氧化铅别名过氧化铅、二氧化铅、氧化高铅,分子式PbO2,不溶于水和醇,易溶于乙酸和氢氧化钠,经过加热会分解。二氧化铅常用于染料、火柴、焰火、合成橡胶、电极等制造,用作氧化剂。可由漂白粉与碱性氢氧化铅溶液作用而得。
所以,配制二氧化铅饱和溶液要用煮沸的水,使水中几乎无氧气或氯气等。氯化铅难溶于冷水,微溶于热水。常温下在水中的溶解度不大,为0.99克/100克水(20℃)。由于它是强酸弱碱盐,为抑制水解作用,在配制其溶液时要用加热煮沸过的蒸溜水,以除去水中溶有的二氧化炭。
应该是两性氧化物,只是酸性表现得比碱性要强,二氧化铅系两性氧化物,酸性比碱性强。跟强碱共热生成铅酸盐。有强氧化性。跟硫酸共热生成硫酸铅、氧气和水。跟盐酸共热,生成二氯化铅、氯气和水。
二氧化铅,以其化学名称O2Pb和英文名Lead dioxide知名,也被称作过氧化铅和二氧化铅(IV)。在化学界,它有一个国际通用的CAS编号1309-60-0,以及EINECS编号215-174-5,这些编码有助于科学家们进行精确的识别和研究。分子式O2Pb揭示了二氧化铅分子的构成,其中氧原子与铅原子以特定的比例结合。
二氧化铅性质与稳定性
1、二氧化铅具有强烈的氧化性质,作为一种危险的化学品,它在加热条件下能够与强碱反应生成高铅酸盐,这种反应是高度放热的,需谨慎操作,因为它具有毒性。二氧化铅在光照下会发生分解,产物是四氧化三铅和氧气,显示出其氧化性。
2、二氧化铅是两性氧化物,酸性比碱性强。与强碱共热能生成铅酸盐,有强氧化性。与硫酸共热生成硫酸铅、氧气和水,与盐酸共热生成二氯化铅、氯气和水。与硫、磷等可燃物混和研磨可引发爆炸。二氧化铅用途广泛,用作分析试剂、氧化剂、媒染剂、蓄电池电极,还用于制火柴、染料等。
3、二氧化铅电极具有电阻率低、化学性质稳定、耐蚀性好、导电性好、可通过大电流等特性,具有三维立体结构涂层(贵金属氧化物+α-PbO2+β-PbO2),大幅度提升了镀层的结合力。
4、这种物质具有一定的溶解性,特别是在酸性环境中,但其相对分子量较大导致其溶解度不高。二氧化铅在工业上有广泛的应用,尤其在电池制造、涂料、玻璃制造等领域中作为重要的原料或添加剂。此外,它也在化学分析中被用作氧化剂或电极材料。
5、过氧化铅的理化性质主要体现在其纯品成分上,表现为棕褐色的结晶或粉末形态。其熔点在290℃时会分解,显示出一定的热稳定性。尽管没有给出具体的沸点数值,但其相对密度相对较高,为38,比水重。在蒸气状态下,其蒸气压和与空气的相对密度信息并未提供。
6、其化学稳定性强,硬度大,但机械强度相对较弱,易碎。在硫酸介质中,钛基二氧化铅阳极表现出优异的性能,常被用于电解工业中的不溶性电极制作。在无机化工领域,钛基二氧化铅阳极的应用广泛。
PbO是氧化铅,那么PbO2是什么
1、PbO:Pb失去两个电子给O,形成离子键。 所以Pb化合价为+2,O化合价为-PbO2:Pb失去两个电子给2个O,形成离子键;但是2个O之间形成共价键,这个与过氧化钠相似。 所以Pb化合价为+2,O化合价为+1。
2、二氧化铅又称棕色氧化铅。英文名称为lead(IV) oxide。化学式PbO2,式量2319,棕色细片粉末。密度375克/厘米3,难溶于水和乙醇。将二氧化铅加热,它会逐步转变为铅的低氧化态氧化物并放出氧气。二氧化铅系两性氧化物,酸性比碱性强。跟强碱共热生成铅酸盐。有强氧化性。
3、一氧化铅---PbO---俗称“弥陀僧”,有红色四方晶体和黄色正交晶体两种变体,常温下红色比较稳定 二氧化铅---PbO2---为黑色粉末,难溶于水的两性氧化物,酸性大于碱性。
4、PBO2的化学名称为二氧化铅。二氧化铅是一种无机化合物,它是氧和铅的化合物,其化学式为PbO2。二氧化铅有多种形态,例如型、型等。它是一种黄色固体,在高温下可以展现出不同的物理性质。这种物质具有一定的溶解性,特别是在酸性环境中,但其相对分子量较大导致其溶解度不高。
5、PbO2,全称为过氧化铅,是一种化学化合物,主要应用于金属制品的表面处理技术中。它的作用是通过镀覆其他金属或者通过化学反应在铁制品表面形成一层致密的氧化膜,例如我们常见的锯条上的烤蓝层。
过氧化铅基本信息
1、过氧化铅的理化性质主要体现在其纯品成分上,表现为棕褐色的结晶或粉末形态。其熔点在290℃时会分解,显示出一定的热稳定性。尽管没有给出具体的沸点数值,但其相对密度相对较高,为38,比水重。在蒸气状态下,其蒸气压和与空气的相对密度信息并未提供。
2、二氧化铅,以其化学名称O2Pb和英文名Lead dioxide知名,也被称作过氧化铅和二氧化铅(IV)。在化学界,它有一个国际通用的CAS编号1309-60-0,以及EINECS编号215-174-5,这些编码有助于科学家们进行精确的识别和研究。分子式O2Pb揭示了二氧化铅分子的构成,其中氧原子与铅原子以特定的比例结合。
3、二氧化铅是一种棕黑色的结晶。二氧化铅别名过氧化铅、二氧化铅、氧化高铅,分子式PbO2,不溶于水和醇,易溶于乙酸和氢氧化钠,经过加热会分解。二氧化铅常用于染料、火柴、焰火、合成橡胶、电极等制造,用作氧化剂。可由漂白粉与碱性氢氧化铅溶液作用而得。
二氧化铅用途与合成方法
二氧化铅用途广泛,用作分析试剂、氧化剂、媒染剂、蓄电池电极,还用于制火柴、染料等。其制备方法多样,如熔融的氯酸钾或硝酸盐氧化一氧化铅,或次氯酸钠氧化亚铅酸盐。二氧化铅具有导电性好、化学稳定性高、硬度大、耐磨损、重量轻、成本低等优点,广泛应用于电化学工业中作为阳极材料。
为纸张增添特有的色泽。在造纸工业中,作为一种黄色素,它被用于提升纸张的外观质量。在印染工业中,硝酸铅作为煤染剂,帮助实现染料的精确应用。在无机工业中,硝酸铅是制造其他铅盐和二氧化铅的关键原料,对于化工生产至关重要。
用作分析试剂、氧化剂、媒染剂、铅酸蓄电池正极的活性物质,还用于制火柴、染料等。用熔融的氯酸钾或硝酸盐氧化一氧化铅(PbO),或用次氯酸钠氧化亚铅酸盐可制得二氧化铅。二氧化铅在自然界中以块状黑铅矿存在。