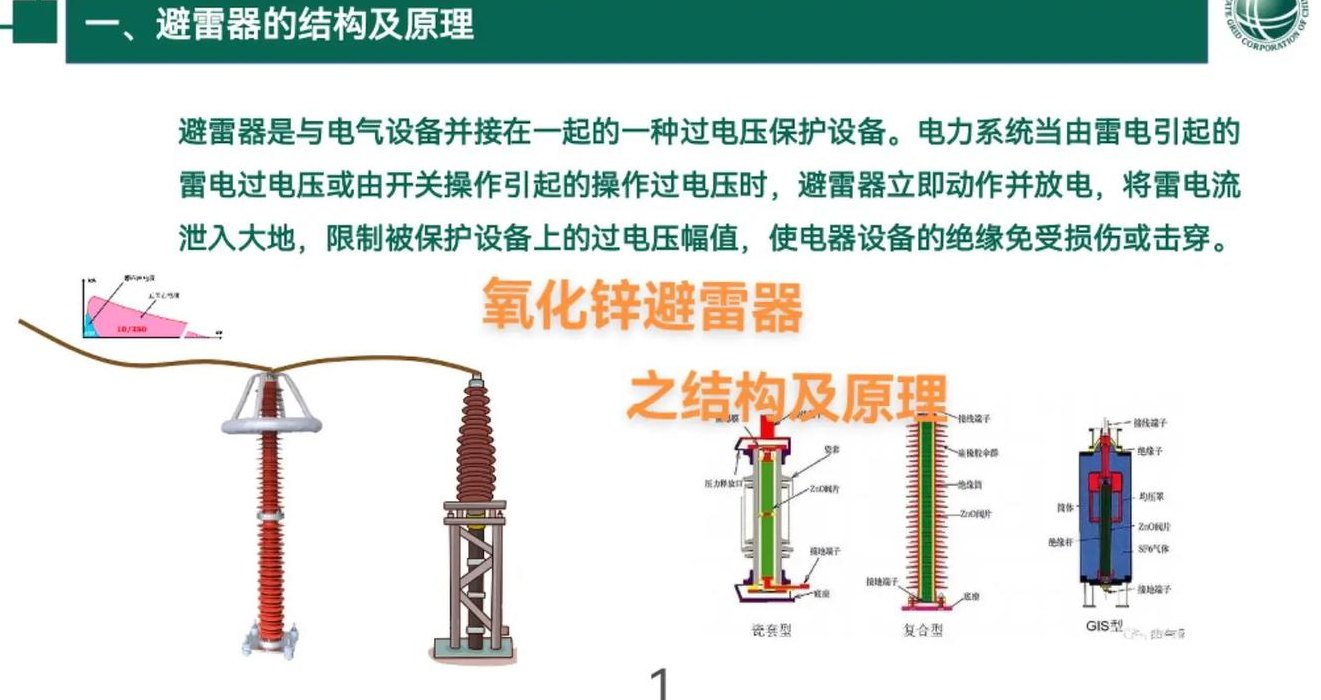
金属氧化物(金属氧化物避雷器的特点包括动作迅速)
金属氧化物的定义
1、金属氧化物是指由金属元素与氧元素结合形成的化合物,这类化合物的典型例子包括钠与氧结合形成的氧化钠(Na2O)。其中,一类特殊的金属氧化物被称为碱性氧化物,它们具有特殊的化学性质。当这类氧化物与酸反应时,会生成相应的盐和水。
2、该氧化物指的是由金属元素与氧元素结合形成的化合物。金属氧化物是氧化物的一种,包括氧化铁(FeO)、氧化铜(CuO)等。氧化物是由氧元素与另一元素结合形成的化合物,可分为金属氧化物和非金属氧化物两大类。
3、金属氧化物是指氧元素与另外一种金属化学元素组成的二元化合物,如氧化铁(FeO)、氧化钠(NaO)等。金属氧化物包括碱性氧化物、酸性氧化物、过氧化物、超氧化物、两性氧化物。金属氧化物在日常生活中应用广泛。
金属氧化物有那些?
1、二价金属氧化物则包括铍氧化物(BeO)、镁氧化物(MgO)、钙氧化物(CaO)、钡氧化物(BaO)、氧化铜(CuO)、锌氧化物(ZnO)和汞氧化物(HgO)。四价金属氧化物有二氧化钛(TiO2)、二氧化锰(MnO2)、四氧化二钒(V2O4)和二氧化铅(PbO2)。
2、O)、氧化钠(NaO)等。金属氧化物包括碱性氧化物、酸性氧化物、过氧化物、超氧化物、两性氧化物。金属氧化物在日常生活中应用广泛。生石灰是一种常用的干燥剂,也可用于消毒;氧化铁(FeO)俗称铁红,可作红色颜料;一些工业过程中应用的催化剂也是金属氧化物。
3、两性金属氧化物有氧化铍、氧化铝、氧化镓、氧化锌、二氧化锗、氧化锑、氧化铋、二氧化钛、二氧化锆等。两性氧化物的组成:主要由活动性较低的金属的氧化物组成。两性氧化物:两性氧化物是指遇强酸呈碱性,遇强碱呈酸性的氧化物,既能与酸作用,又能与碱作用。都生成盐和水。
4、金属氧化物中,部分不是电解质。以下是一些不是电解质的金属氧化物: 氧化铁(FeO)。在常温常压下,氧化铁不能形成离子,因此不能导电。虽然它在水中的溶解度很小,但溶解的部分能完全电离出离子,所以它是电解质。
5、活泼金属氧化物包括氧化钠、氧化钾、氧化钙、氧化镁、氧化铝等。以下是针对活泼金属氧化物的详细解释: 活泼金属氧化物定义:活泼金属氧化物指的是那些由活泼金属元素与氧元素结合而成的化合物。这些金属通常在常温下易于与氧气反应,形成稳定的氧化物。
金属氧化物有哪些
1、对于一价金属氧化物,常见的有锂氧化物(Li2O)、钠氧化物(Na2O)、钾氧化物(K2O)、银氧化物(Ag2O)和氧化亚铜(Cu2O)。二价金属氧化物则包括铍氧化物(BeO)、镁氧化物(MgO)、钙氧化物(CaO)、钡氧化物(BaO)、氧化铜(CuO)、锌氧化物(ZnO)和汞氧化物(HgO)。
2、碱金属氧化物(如氢氧化钠、氢氧化钾):这些氧化物都是强碱,能够与水反应生成氢氧化物离子(OH-)。因此,碱金属氧化物可以溶于水并形成碱性溶液。碱土金属氧化物(如氢氧化钙、氢氧化镁):这些氧化物的溶解度较低,但在一定程度上可以溶解于水。
3、两性金属氧化物有氧化铍、氧化铝、氧化镓、氧化锌、二氧化锗、氧化锑、氧化铋、二氧化钛、二氧化锆等。两性氧化物的组成:主要由活动性较低的金属的氧化物组成。两性氧化物:两性氧化物是指遇强酸呈碱性,遇强碱呈酸性的氧化物,既能与酸作用,又能与碱作用。都生成盐和水。
4、不一定,有的金属氧化物是酸性氧化物,比如Mn2OWOPbO2,它们不能与酸反应,只溶于强碱。酸可以与金属氧化物中的碱性氧化物以及两性氧化物反应生成盐和水。碱性氧化物如MgO、BaO等,两性氧化物如Al2O、ZnO等3。与金属氧化物中的酸性氧化物没有酸碱反应,如Mn2OCrO3等。