原电池负极发生什么反应(原电池负极发生的反应)
如何写原电池电极反应式。
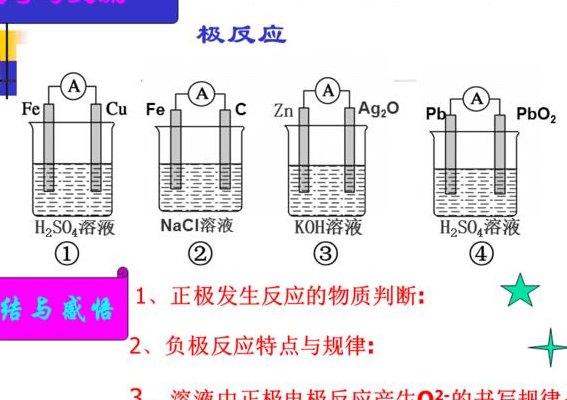
由于在反应中氧气由0价变为-2价,所以肯定是O2得电子,即O2作氧化剂是正极,即可写出正极的电极反应式:O2+4e-+2H2O=4OH-①(该反应式为常见的绝大多数燃料电池的正极反应式)。
正负号写在最两边,即“(-)”写在最左边,“(+)”写在最右边。里面一层一般写与外界导线相连的相。再里面一层写其他相。中间用双竖线“||”表示盐桥。相与相之间用逗号“,”或单竖线“|”分割。有分界面的两相用单竖线分割。
电极反应式怎么写 根据总反应写原电池各电极反应式方法:先写负极反应式,先要考虑还原剂失电子生成什么离子,然后考虑生成离子是否会和电解质溶液反应,再结合总反应中生成物写出负极反应式.再用总反应方程式(要写成离子方程式)减去负极反应式就得到了正极反应式。
原电池负极发生什么反应
1、原电池放电时,负极发生氧化反应,正极发生还原反应。例如铜锌原电池又称丹尼尔电池,其正极是铜极,浸在硫酸铜溶液中;负极是锌板,浸在硫酸锌溶液中。两种电解质溶液用盐桥连接,两极用导线相连就组成原电池。
2、原电池的负极发生氧化反应,金属失去电子。在原电池中,发生的化学反应是氧化还原反应。发生氧化反应的一极上有电子流出,做负极,失去电子的物质是还原剂。电子通过原电池的负极经导线流向正极,在正极上氧化剂得到电子,发生还原反应。原电池就是通过化学反应实现化学能向电能转化的。
3、满意答案 热心问友 2011-08-16负极是失去电子被氧化,发生氧化反应,如:在构成的原电池(镁和碳中)Mg+2H+=Mg2++H2^中镁作负极,碳作正极 追问: 为何会失去电子。
4、正负极的判断方法:负极发生氧化反应,失电子;正极发生还原反应,得到电子。
原电池为什么有的负极和OH-反应,有的却不反应?
1、这是因为原电池分为析氢反应和吸氧反应。根据原电池原理可得:负极:失电子 发生氧化反应(一般通式:M Mn+ + ne-) 正极:得电子 发生还原反应(一般通式:N + me- Nm-) 要把电极反应式准确写出,最关键的是把握准总反应。负极发生放电反应,也就是失去电子,发生了氧化反应。
2、一种是负极金属失电子后生成金属阳离子不与电解质溶液的成分反应,此时是电极反应可表示为M-ne-=Mn+。
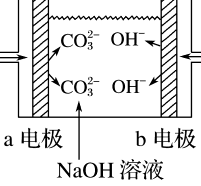
3、放电为原电池,充电为电解池。那要看电解质的酸碱性了,若电极为碱性物质而电解质溶液呈酸性那就要考虑反应,例如 Pd作电极,一极通入C3H8另一极通入空气用KOH作电解质那么 C3H8+5O2===3CO2+4H2O(CO2+2OH- ===CO3^2- +H2O)此时就要考虑与电解质的反应了。有问题的话可以继续问。。
4、负极Zn失电子形成Zn2+,与OH-结合形成弱碱氢氧化锌,消耗了OH-。因此pH减小。铜锌原电池是Zn与H+的反应,硫酸根属于无关离子,不参与反应,因此它不会特别向某一极移动,两极浓度相等。正极反应物一般不是材料。就像Zn-Cu的硫酸原电池,Cu是不反应的。
5、碱性条件下,正极附近没有氢离子,因此氢氧根不会生成水,所以正极生成的是氢氧根。酸性条件下,负极生成氢离子,因为原电池中正极会吸引阳离子,所以氢氧根和氢离子反应生成水。高中都是这么理解的。