饱和碳酸氢钠(饱和碳酸氢钠浓度)
请问常温下碳酸氢钠的饱和度是多少?
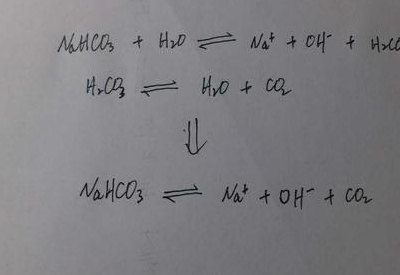
常温常压下饱和碳酸钠的PH为16;碳酸氢钠的pH值为3。碳酸氢钠是强碱与弱酸中和后生成的酸式盐,溶于水时呈现弱碱性。此特性可使其作为食品制作过程中的膨松剂。碳酸氢钠在作用后会残留碳酸钠,使用过多会使成品有碱味。
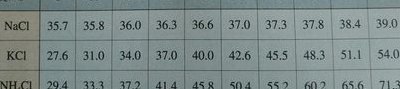
查了各种资料后,发现常温下饱和碳酸钠溶液的ph值是12左右,而夏天30℃碳酸钠的溶解度是37g/100g水,大概比例是1:3左右。那么取食用碱1:3溶于水后,过滤可以获得。比如说2克枧水,就是用0.5克的纯碱粉和5克的水混合就可以了。
标准碳酸氢根(AB)是指在37℃的条件下,动脉血中的二氧化碳分压为40mmHg,氧饱和度为100%时测得的碳酸氢根含量。成人的正常值范围在22至27mmol/L之间,而儿童则在21至25mmol/L之间。成人碳酸氢钠(SB)的正常值范围为21至25mmol/L。在正常情况下,碳酸氢钠的含量大致等于碳酸氢根的含量。
饱和的碳酸氢钠溶液的作用
1、饱和碳酸氢钠溶液的作用如下:作为缓冲溶液:碳酸氢钠是一种弱碱强酸盐,因此饱和碳酸氢钠溶液可以作为缓冲溶液,提供一定范围的pH值,稳定实验环境中的酸碱度。沉淀剂和清洗剂:饱和碳酸氢钠溶液可以作为沉淀剂,用于沉淀一些金属离子,如钡、锶等。
2、饱和的碳酸氢钠的主要作用是除杂和洗气等。根据百度健康平台显示,饱和的碳酸氢钠用来除去二氧化碳中少量的二氧化硫,一般用于气体的除杂等。去除二氧化碳气体中含有的氯化氢气体,一般用碳酸钙、氯化氢制取二氧化碳后的洗气。饱和碳酸钠溶液可以除去乙酸乙酯中的乙酸。
3、①饱和碳酸氢钠溶液的作用:作用一:洗气CO2,去除CO2气体中含有的HCl气体。一般用于CaCOHCl制取CO2后的洗气。作用二:洗气CO去除CO2气体中含有的SO2气体。一般用于气体的除杂等。
饱和碳酸氢钠沸点
饱和碳酸氢钠的沸点是851℃(1800℉)。饱和碳酸氢钠,也称为重碳酸氢钠,是一种白色固体,化学式为NaHCO3。是一种无机化合物,以晶体的形式存在。饱和碳酸氢钠可以用作食品添加剂,例如在制作糕点、饮料和冰淇淋时,可以用作发酵剂和膨松剂。
度。饱和碳酸氢钠溶液的沸点取决于溶液的浓度。在常压下,饱和碳酸氢钠溶液的沸点为100度。然而,在高压条件下,溶液的沸点会有所提高。
度。根据资料显示,饱和碳酸氢钠的沸点大概是60度,一加热就会分解为碳酸钠、水和CO2。碳酸氢钠,分子式为NaHCO?,是一种无机化合物,呈白色结晶性粉末,无臭,味咸,易溶于水。在潮湿空气或热空气中即缓慢分解,产生二氧化碳,加热至270℃完全分解。
碳酸氢钠的溶液为什么是饱和的
产生浑浊或沉淀的原因不是产生的碳酸氢钠不溶于水,而是因为碳酸氢钠溶液达到了饱和,不能溶解的碳酸氢钠沉淀了下来。达到(化学)平衡的溶液便不能容纳更多的溶质(当然,其他溶质仍能溶解),称之为饱和溶液。碳酸钠易溶于水和甘油。
因为二氧化碳是一种可溶性气体,它在水中溶解的方程式:CO2+H2O=H2CO3=H+ +HCO3- 而饱和碳酸氢钠溶液含有大量HCO3-,可以尽可能地抑制CO2的溶解,而普通的碳酸氢钠溶液做不到这一点。
盐酸溶于水,电离出氢离子,而氢离子与碳酸氢根反应,实验中要除杂时要过量,用饱和就是为了过量,使盐酸能被完全吸收,不过这里需注意一点,盐酸会与碳酸氢钠生成二氧化碳,要考虑生成的二氧化碳是否会有影响。
酯化反应为什么要用饱和碳酸氢钠溶液
此实验中饱和碳酸钠溶液的作用我们通常表述为:吸收乙醇、中和乙酸、降低酯的溶解度,便于酯的分层和闻到酯的香味。即碱性除酸、饱和液易分层。饱和碳酸钠溶液的PH约为6左右,不加热不会水解。
之所以要用饱和碳酸钠溶液是因为:溶解乙醇 中和乙酸 降低乙酸乙酯在水中的溶解度。碳酸氢钠本身在水中的溶解度就小于碳酸钠的 用碳酸氢钠达不到实验效果。
因为碳酸钠的溶解度更好。而且碳酸氢钠中和乙酸的能力比碳酸钠差好多。酯化反应,是一类有机化学反应,是醇跟羧酸或含氧无机酸生成酯和水的反应。分为羧酸跟醇反应和无机含氧酸跟醇反应和无机强酸跟醇的反应三类。羧酸跟醇的酯化反应是可逆的,并且一般反应极缓慢,故常用浓硫酸作催化剂。
盐酸溶于水,电离出氢离子,而氢离子与碳酸氢根反应,实验中要除杂时要过量,用饱和就是为了过量,使盐酸能被完全吸收,不过这里需注意一点,盐酸会与碳酸氢钠生成二氧化碳,要考虑生成的二氧化碳是否会有影响。
碳酸氢钠饱和溶液怎么配制怎么配制碳酸氢钠饱和溶液
1、向水中加入足量的碳酸氢钠固体直到无法再溶解,所得的一定是饱和碳酸氢钠溶液;或者向饱和碳酸钠溶液中通入足量的二氧化碳也会获得饱和的碳酸氢钠溶液。如有碳酸氢钠固体,直接配。若没有,则先配饱和碳酸钠溶液,再向其通入足量二氧化碳。
2、首先,要配制饱和碳酸氢钠溶液,您需要准备一些碳酸氢钠粉末和足够的纯净水。为了避免受到外部物质的污染,最好使用蒸馏水或去离子水等高纯水来配制碳酸氢钠溶液。接下来,将需要的水加入到一个干净的容器中。然后,将碳酸氢钠粉末逐渐加入到水中,并同时搅拌溶解,直到碳酸氢钠大量溶解在水中。
3、加入一小部分蒸馏水,并使用搅拌棒充分搅拌,直到碳酸氢钠完全溶解。逐渐向容量瓶中加入剩余的蒸馏水,搅拌均匀,直到溶液体积接近容量瓶的刻度线。使用均质器或其他方法将溶液均匀混合,确保溶液中的碳酸氢钠分布均匀。最后,通过添加或减少蒸馏水的体积,调整溶液的体积,使其准确达到所需的最终体积。
4、ml饱和碳酸氢钠溶液需要85到19克的碳酸氢钠。因为根据查询相关资料信息实验家实验证明在20到40摄氏度的环境下,100g水里能溶解85到19克的碳酸氢钠,碳酸氢钠的溶解度随温度的变化而变化,起伏明显。
5、碳酸钠易溶于水和甘油。20℃时每一百克水能溶解20克碳酸钠,34℃时溶解度最大,100克水中可溶解47克碳酸钠,微溶于无水乙醇,难溶于丙醇。碳酸氢钠为白色晶体,或不透明单斜晶系细微结晶。比重15。无臭、无毒、味咸,可溶于水,微溶于乙醇。25℃时溶于10份水,约18℃时溶于12份水。
6、这意味着,如果你需要创建一个基础的碱性环境,只需在100毫升水中加入少量小苏打,如超过1克,就足以满足你的需求,无需过度添加。然而,计算溶液的pH值时,通常使用的是摩尔浓度,而非质量分数。例如,一个0.1摩尔每升(0.1M)的碳酸氢钠溶液其pH值约为3。